磷是金属配位化学中的一种核心元素,含磷手性配体在催化合成范式中,可灵活调控过渡金属的催化活性及立体选择性。如何高效构建这一系列磷属化合物,一直以来都是研究热点。其中,手性膦配体及其磷氧衍生物已有较为成熟的合成途径,且两者之间亦有完备的相互转化策略,而类似的手性磷硫化合物却甚少报导较为直接的构建方案。从合成子的角度而言,磷硫双键可藉由更为温和的反应条件转化为相应的膦配体或者磷氧双键,可作为重要的补充使这三者之间形成更为紧密的闭环。从合成角度而言,R2P(=S)H自然存在R2P-SH的互变异构式,这也是最终参与成键历程的亲核物种,以非共价活化机制激活反应的催化剂,需提供稳健的氢键相互作用,将亲核试剂限定于该有的反应状态,且形成具有精准空间密码结构的过渡态,以实现后续反应的面选择性控制。2014年,由黄湧/陈杰安课题组首次实现氮杂环卡宾(N‑heterocyclic carbenes, NHCs)的非共价活化机制(Nat. Commun. 2014, 5, 3437),并逐步实现脂肪硫醇、脂肪胺的不对称共轭加成反应(Angew. Chem. Int. Ed. 2015, 54, 15414; Chem. Sci. 2015, 6, 4184; Sci. China Chem. 2016, 59, 251; N-Heterocyclic Carbenes in Organocatalysis, Wiley-VCH, Weinheim, 2019, 261-286),于近期亦初次提出NHC与氢键供体(H-Bonding Donor, HBD)嵌合体的概念,实现双取代胺类亲核试剂的不对称共轭加成反应(ACS Catal. 2021, 11, 6316)。于此,项目组利用NHC作为手性Brønsted碱催化剂,活化双芳基磷硫化合物,以手性联萘酚作为氢键供体活化硝基烯烃底物,通过双活化模式实现不对称phospha-Michael加成反应,构建一系列α-手性磷硫化合物,并尝试以温和反应条件实现与膦化合物及磷氧衍生物的转化,相关成果在线发表在Cell Reports Physical Science上(Cell Rep. Phy. Sci., 2021, 2, 100490. DOI: 10.1016/j.xcrp.2021.100490)。
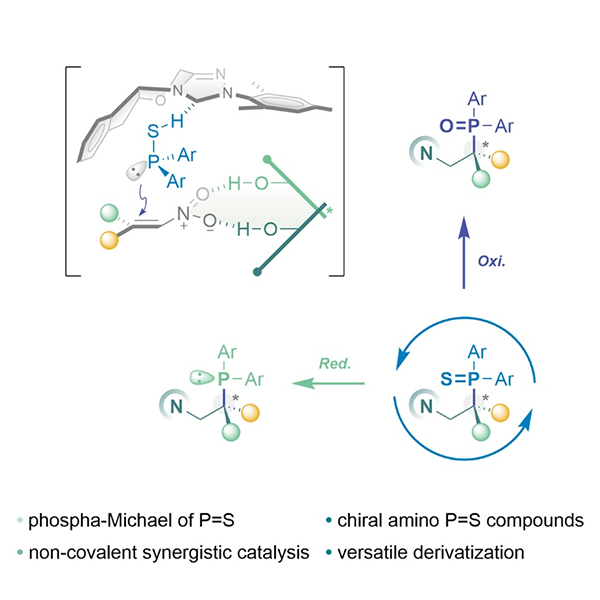
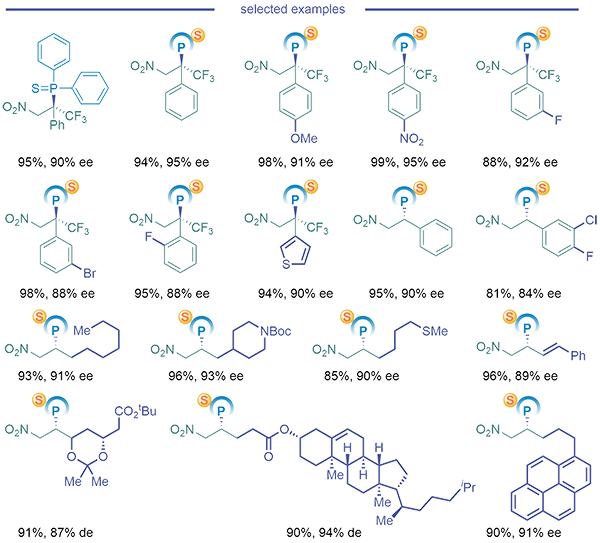
通过机理实验,证明手性氢键催化剂R-BINOL两个羟基的必要性,可同时提高反应的转化效率及对映选择性。在底物的普适性考察中,β-芳基硝基烯烃均能以优异的产率及ee值得到目标产物;具有β-芳基-β-CF3基团的底物也具有良好耐受性,可以合成独特的同时含P、CF3的季碳手性中心;对较少出现于不对称phospha-Michael反应范畴的β-烷基硝基烯烃系列,利用这一协同的非共价活化机制亦可获得较优的转化率及对映选择性。对于官能团容忍性的考察,整体而言具有较大的适应图谱,对于较为复杂的活性分子片段,经由简单的预修饰,亦可快速引入这一特殊的α-手性磷硫位点,预期在潜药分子的后期修饰中有一定的应用价值。
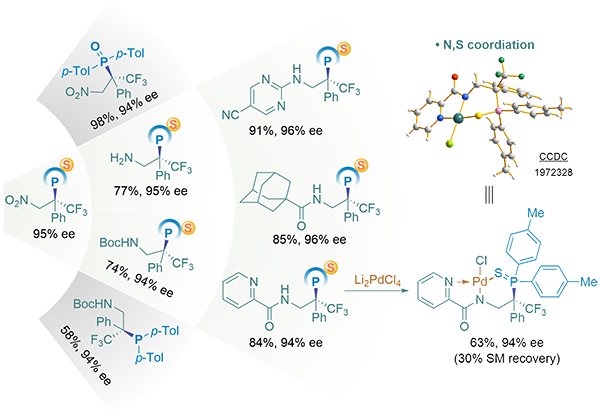
衍生化方面,手性α-CF3磷硫化合物可经由温和反应条件,转化为相应的手性膦配体及磷氧衍生物,手性可完全传递。加成产物连带的硝基可高效还原为自由氨基,组建特殊的1,2-氨基磷硫化合物,其间包括了具有α,α-CF3,P手性中心的衍生物,从而串联各种修饰氨基修饰以制备潜在的多螯合位点金属配体。在于金属钯的初步螯合实验中,项目组成功合成一种κ3-NNS-Pd复合物,该化合物于单晶结构中呈现刚性的钳型5,6-环钯并环结构,初步展示此类别化合物作为过渡金属手性配体的应用场景,后续衍生化研究以及配位化学、催化性质等方面的延展正在推进。
以上工作由香港科技大学黄湧教授/深圳湾实验室陈杰安研究员共同指导,由北京大学深圳研究生院博士研究生李恩、王骞、蔡雨兴合作完成,依托于省部共建肿瘤化学基因组学国家重点实验室,得到了国家自然科学基金委员会、广东省自然科学基金委员会、深圳市科技创新委员会和香港研究资助局的资助。(文字:陈杰安/李恩)

